Anyar-anyar ieu, tilu obat terapi gen parantos disatujuan pikeun pamasaran, nyaéta: (1) Dina 21 Juli 2022, PTC Therapeutics, Inc. (NASDAQ: PTCT) ngumumkeun yén terapi gen AAV na Upstaza™ disatujuan ku Komisi Éropa.(2) Dina 17 Agustus 2022, Administrasi Pangan sareng Narkoba AS (FDA) nyatujuan terapi gen Bluebird Bio Zynteglo (betibeglogene autotemcel, beti-cel) pikeun pengobatan talasemia béta.Persetujuan terapi di Amérika Serikat pasti mangrupikeun "pitulung dina salju" pikeun Bluebird Bio, anu aya dina krisis finansial.(3) Dina 24 Agustus 2022, BioMarin Pharmaceutical (BioMarin) ngumumkeun yén Komisi Éropa nyatujuan pamasaran kondisional ROCTAVIAN™ (valoctocogene roxaparvovec), terapi gén pikeun hemofilia A, pikeun pengobatan pasien anu henteu aya riwayat inhibitor faktor FVIII sareng antibodi AAV5 négatip AAV5 pikeun pasien déwasa anu disatujuan pikeun Hemofilia Hemophilia parna.Sajauh ieu, 41 ubar terapi gen parantos disatujuan pikeun pamasaran di sakuliah dunya.
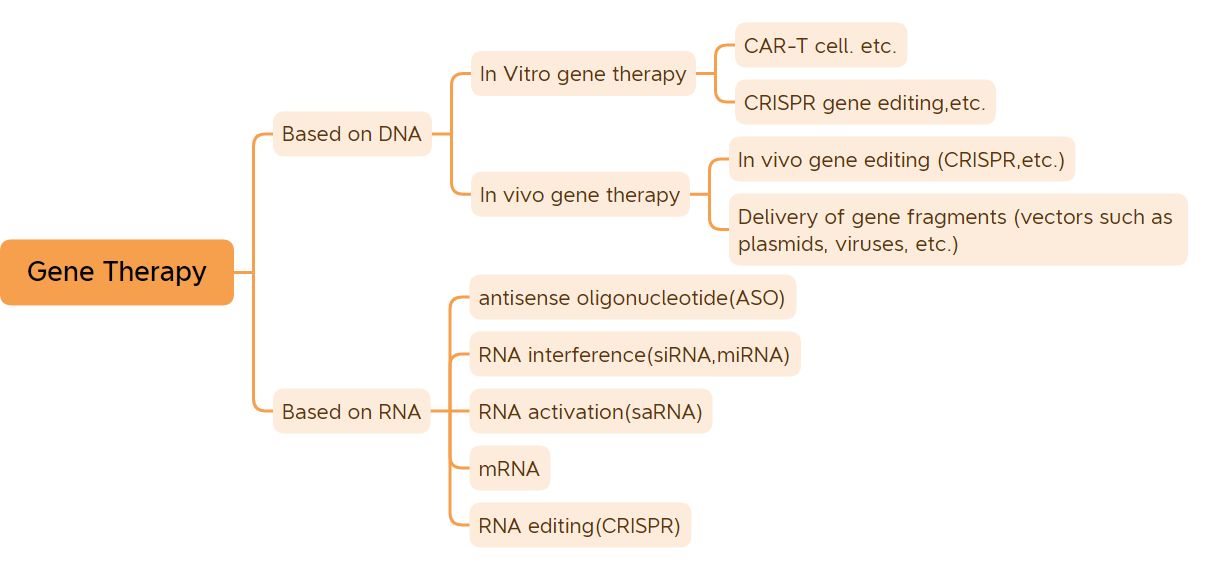
Gén nyaéta unit genetik dasar anu ngatur sipat.Iwal gén sababaraha virus, nu diwangun ku RNA, gén lolobana organisme diwangun ku DNA.Kaseueuran panyakit organisme disababkeun ku interaksi antara gén sareng lingkungan, sareng seueur panyakit anu tiasa diubaran atanapi diréduksi dina hakekatna ngalangkungan terapi gen.Terapi gén dianggap révolusi dina widang kadokteran sareng apoték.Ubar terapi gen anu lega kalebet ubar dumasar kana ubar DNA anu dimodifikasi DNA (sapertos obat terapi gén vivo berbasis vektor virus, obat terapi gen in vitro, obat plasmid taranjang, jsb.) sareng obat RNA (sapertos obat antisense oligonucleotide, obat siRNA, sareng terapi gén mRNA, jsb.);obat terapi gen diartikeun heureut utamana ngawengku ubar DNA plasmid, ubar terapi gén dumasar kana vektor viral, ubar terapi gén dumasar kana vektor baktéri, sistem édit gén jeung ubar terapi sél nu dirobah genetik in vitro.Sanggeus taun ngembangkeun tortuous, ubar terapi gén geus ngahontal hasil klinis mereun.(kaasup vaksin DNA jeung vaksin mRNA), 41 ubar terapi gén geus disatujuan pikeun pamasaran di dunya.Kalayan peluncuran produk sareng pamekaran gancang téknologi terapi gén, terapi gén badé ngiringan periode pangembangan anu gancang.
Klasifikasi terapi gén (Sumber gambar: Jingwei Biologis)
Artikel ieu daptar 41 terapi gén nu geus disatujuan pikeun pamasaran (teu kaasup vaksin DNA jeung vaksin mRNA).
1. Terapi gén in vitro
(1) Strimvelis
Perusahaan: Dimekarkeun ku GlaxoSmithKline (GSK).
Waktos ka pasar: Disatujuan ku Uni Éropa dina Méi 2016.
Indikasi: Pikeun pengobatan immunodeficiency gabungan parna (SCID).
Catetan: Prosés umum terapi ieu mimitina ménta sél stém hematopoietik sabar urang sorangan, dilegakeun tur budaya aranjeunna in vitro, lajeng nganggo retrovirus pikeun ngawanohkeun salinan gén ADA (adénosin deaminase) fungsi kana sél stém hematopoietik maranéhanana, sarta tungtungna mindahkeun sél stém hematopoietik dirobah.Sél stém hématopoétik diinfuskeun deui kana awak.Hasil klinis nunjukkeun yén tingkat survival 3 taun pasien ADA-SCID anu dirawat kalayan Strimvelis nyaéta 100%.
(2) Zalmoxis
pausahaan: Dihasilkeun ku MolMed, Italia.
Waktos ka pasar: Kéngingkeun otorisasi pamasaran kondisional EU di 2016.
Indikasi: Hal ieu dipaké pikeun terapi adjuvant tina sistim imun pasien sanggeus cangkok sél stém hematopoietic.
Catetan: Zalmoxis mangrupikeun immunotherapy gén bunuh diri sél T allogénik anu dirobih ku véktor retroviral.The 1NGFR na HSV-TK Mut2 gén bunuh diri ngidinan jalma ngagunakeun ganciclovir iraha wae pikeun maéhan sél T anu ngabalukarkeun réspon imun ngarugikeun, nyegah deterioration salajengna tina GVHD anu bisa lumangsung, sarta malikkeun fungsi imun di penderita HSCT haploidentical sanggeus bedah Ngiringan.
(3) Invossa-K
pausahaan: Dimekarkeun ku TissueGene (KolonTissueGene) pausahaan.
Waktos ka pasar: Disatujuan pikeun daptar di Koréa Kidul dina Juli 2017.
Indikasi: Pikeun pengobatan rematik degeneratif dengkul.
Catetan: Invossa-K mangrupikeun terapi gén sél alogénik anu ngalibatkeun kondrosit manusa.Sél alogénik dirobih sacara genetik in vitro, sareng sél anu dirobih tiasa nganyatakeun sareng ngaluarkeun faktor pertumbuhan transformasi β1 (TGF-β1) saatos suntikan intra-artikular.β1), sahingga ningkatkeun gejala osteoarthritis.Hasil klinis nunjukkeun yén Invossa-K tiasa sacara signifikan ningkatkeun rematik dengkul.Lisénsi éta dicabut ku régulator ubar Koréa Kidul dina taun 2019 kusabab produsén henteu leres-leres nyetel bahan anu dianggo.
(4) Zynteglo
Perusahaan: Dimekarkeun ku Amérika bluebird bio (bluebird bio) parusahaan.
Waktos ka pasar: Disatujuan ku Uni Éropa dina 2019, sareng disatujuan ku FDA dina Agustus 2022.
Indikasi: Pikeun pengobatan β-thalassemia gumantung transfusi.
Catetan: Zynteglo mangrupikeun terapi gén in vitro lentiviral, anu ngagunakeun véktor lentiviral pikeun ngawanohkeun salinan fungsional gén β-globin normal (gén βA-T87Q-globin) kana sél stém hematopoietik anu dikaluarkeun tina pasien., lajeng infuse ieu dirobah genetik sél stém hematopoietic autologous deui kana sabar.Sakali pasien ngagaduhan gén globin βA-T87Q-globin normal, aranjeunna tiasa ngahasilkeun protéin HbAT87Q normal, anu sacara efektif tiasa ngirangan atanapi ngaleungitkeun kabutuhan transfusi getih.Ieu mangrupikeun terapi sakali-waktos anu dirancang pikeun ngagentos transfusi getih seumur hirup sareng pangobatan seumur hirup pikeun pasien umur 12 taun sareng langkung lami.
(5) Skysona
Perusahaan: Dimekarkeun ku Amérika bluebird bio (bluebird bio) parusahaan.
Waktos ka pasar: Disatujuan ku EU pikeun pamasaran dina Juli 2021.
Indikasi: Pikeun pengobatan awal adrenoleukodystrophy cerebral (CALD).
Catetan: Terapi gén Skysona mangrupikeun hiji-hijina terapi gen anu disatujuan pikeun pengobatan awal adrenoleukodystrophy cerebral (CALD).Skysona (elivaldogene autotemcel, Lenti-D) mangrupikeun lentiviral sél stém hematopoietik dina terapi gen vitro Lenti-D.Prosés umum terapi nyaéta kieu: sél stém hematopoietik autologous dicokot kaluar ti sabar, dirobah in vitro ku lentivirus mawa gén ABCD1 manusa, lajeng infused deui ka sabar.Pikeun pengobatan pasien di handapeun umur 18 kalayan mutasi gen ABCD1 sareng CALD.
(6) Kymriah
pausahaan: Dimekarkeun ku Novartis.
Waktos ka pasar: Disatujuan ku FDA dina Agustus 2017.
Indikasi: Perlakuan prékursor B-sél leukemia lymphoblastic akut (ALL) jeung DLBCL kambuh jeung refractory.
Catetan: Kymriah mangrupikeun ubar terapi gén in vitro lentiviral, terapi CAR-T anu munggaran disatujuan di dunya, nargétkeun CD19 sareng nganggo faktor stimulasi ko-4-1BB.Hargana $475,000 di AS sareng $313,000 di Jepang.
(7) Yescarta
Perusahaan: Dimekarkeun ku Kite Pharma, anak perusahaan Gilead.
Waktos ka pasar: Disatujuan ku FDA dina Oktober 2017.
Indikasi: Pikeun pengobatan kambuh atanapi refractory lymphoma-sél B badag.
Catetan: Yescarta mangrupikeun terapi gén in vitro retroviral.Éta mangrupikeun terapi CAR-T kadua anu disatujuan di dunya.Éta nargétkeun CD19 sareng nganggo faktor kostimulasi CD28.Harga di AS nyaéta $373,000.
(8) Tecartus
Perusahaan: Dimekarkeun ku Gilead (GILD).
Waktos ka pasar: Disatujuan ku FDA dina Juli 2020.
Indikasi: Pikeun limfoma sél mantel kambuh atanapi refractory.
Catetan: Tecartus mangrupikeun terapi sél CAR-T autologous nargétkeun CD19, sareng mangrupikeun terapi CAR-T katilu anu disatujuan pikeun pamasaran di dunya.
(9) Breyanzi
pausahaan: Dimekarkeun ku Bristol-Myers Squibb (BMS).
Waktos ka pasar: Disatujuan ku FDA dina bulan Pebruari 2021.
Indikasi: Kambuh atanapi refractory (R / R) lymphoma sél B badag (LBCL).
Catetan: Breyanzi mangrupikeun terapi gén in vitro dumasar kana lentivirus, sareng terapi CAR-T kaopat disatujuan pikeun pamasaran di dunya, nargétkeun CD19.Persetujuan Breyanzi mangrupikeun tonggak penting pikeun Bristol-Myers Squibb dina widang immunotherapy sélular, anu dicandak ku Bristol-Myers nalika kaala Celgene $ 74 milyar taun 2019.
(10) Abecma
pausahaan: Co-dimekarkeun ku Bristol-Myers Squibb (BMS) jeung bluebird bio.
Waktos ka pasar: Disatujuan ku FDA dina Maret 2021.
Indikasi: kambuh atanapi refractory multiple myeloma.
Catetan: Abecma mangrupikeun terapi gén in vitro berbasis lentivirus, terapi sél CAR-T munggaran di dunya anu nargétkeun BCMA, sareng terapi CAR-T kalima anu disatujuan ku FDA.Prinsip ubar nyaéta pikeun nganyatakeun reséptor BCMA chimeric dina sél T autologous pasien ngaliwatan modifikasi genetik dimédiasi lentivirus in vitro.Sateuacan infus ubar gen sél, pasien nampi dua sanyawa cyclophosphamide sareng fludarabine pikeun pre-treatment.Perlakuan pikeun miceun sél T unmodified ti sabar, lajeng infuse sél T dirobah deui kana awak sabar urang pikeun neangan kaluar sarta maéhan sél kanker BCMA-ekspresi.
(11) Libmeldy
Perusahaan: Dimekarkeun ku Orchard Therapeutics.
Waktos ka pasar: Disatujuan ku Uni Éropa pikeun daptar dina Désémber 2020.
Indikasi: Pikeun pengobatan leukodystrophy metachromatic (MLD).
Catetan: Libmeldy mangrupikeun terapi gen dumasar kana modifikasi gén in vitro lentiviral tina sél CD34+ autologous.Data klinis nunjukkeun yén hiji infus intravena tunggal Libmeldy mujarab pikeun ngarobih kursus MLD awal-awal sareng gangguan motor sareng kognitif parah dina pasien anu henteu dirawat dina umur anu sami.
(12) Benoda
pausahaan: Dimekarkeun ku WuXi Junuo.
Waktos ka pasar: Disatujuan sacara resmi ku NMPA dina Séptémber 2021.
Indikasi: Perlakuan lymphoma-sél B badag kambuh atawa refractory (r / r LBCL) dina penderita sawawa sanggeus kadua-garis atawa terapi leuwih sistemik.
Catetan: Benoda mangrupikeun terapi gén anti CD19 CAR-T, sareng éta ogé produk inti WuXi Junuo.Ieu produk CAR-T kadua disatujuan di Cina, iwal lymphoma sél B badag kambuh / refractory.Salaku tambahan, WuXi Junuo ogé ngarencanakeun pikeun ngembangkeun suntikan Ruiki Orenza pikeun pengobatan rupa-rupa indikasi anu sanés, kalebet limfoma follicular (FL), limfoma sél mantel (MCL), leukemia limfositik kronis (CLL), limfoma sél B ageung diffuse garis kadua (DLBCL) sareng leukemia limfoblastik akut (ALL).
(13) CARVYKTI
pausahaan: produk munggaran disatujuan Legenda Bio urang.
Waktos ka pasar: Disatujuan ku FDA dina bulan Pebruari 2022.
Indikasi: Perawatan sababaraha myeloma kambuh atanapi refractory (R / R MM).
Catetan: CARVYKTI (ciltacabtagene autoleucel, disebut Cilta-cel) nyaéta terapi gén imun sél CAR-T kalawan dua antibodi domain tunggal nargétkeun antigen maturation sél B (BCMA).Data nunjukkeun yén CARVYKTI nunjukkeun tingkat réspon sadayana dugi ka 98% dina pasien anu kambuh atanapi refractory multiple myeloma anu nampi opat atanapi langkung terapi sateuacana, kalebet inhibitor proteasome, immunomodulators, sareng antibodi monoklonal anti CD38.
2. Terapi gén in vivo dumasar kana vektor viral
(1) Gendicine/dilahirkeun deui
Perusahaan: Dimekarkeun ku Shenzhen Saibainuo Company.
Waktos ka pasar: Disatujuan pikeun daptar di Cina di 2003.
Indikasi: Pikeun pengobatan carcinoma sél squamous tina sirah jeung beuheung.
Catetan: Rekombinan manusa p53 adenovirus suntik Gendicine / Jinshengsheng mangrupakeun ubar terapi gén vektor adenovirus kalawan hak cipta intelektual bebas milik Shenzhen Saibainuo Company.Ubar ieu diwangun ku gén suppressor tumor manusa normal p53 jeung rékombinan jieunan réplikasi-kakurangan Asasi Manusa adenovirus tipe 5 diwangun ku tipe adenovirus manusa 5. Urut mangrupa struktur utama ubar pikeun exert pangaruh anti tumor, sarta dimungkinkeun utamana tindakan minangka carrier a.Vektor adenovirus mawa gén terapi p53 kana sél target, sarta expresses tumor suppressor gén p53 dina sél target.produk nu bisa up-ngatur rupa gén anti kanker jeung handap-ngatur kagiatan rupa onkogén, kukituna enhancing pangaruh anti tumor awak sarta achieving tujuan killing tumor.
(2) Rigvir
Perusahaan: Dimekarkeun ku perusahaan Lativia Latima.
Waktos ka pasar: Disatujuan di Latvia dina 2004.
Indikasi: Pikeun pengobatan melanoma.
Catetan: Rigvir mangrupikeun terapi gén dumasar kana véktor enterovirus ECHO-7 anu dimodifikasi gén, anu parantos dianggo di Latvia, Estonia, Polandia, Arménia, Bélarus sareng tempat-tempat sanés, sareng ogé didaptarkeun ka EMA Uni Éropa..Kasus klinis dina sapuluh taun katukang parantos ngabuktikeun yén virus oncolytic Rigvir aman sareng efektif, sareng tiasa ningkatkeun tingkat kasalametan pasien melanoma ku 4-6 kali.Sajaba ti éta, terapi ogé cocog pikeun rupa-rupa kangker lianna, kaasup kanker kolorektal, kanker pankréas, kanker kandung kemih.kanker, kanker ginjal, kanker prostat, kanker paru, kanker uterus, lymphosarcoma, jsb.
(3) Oncorine / Ankerui
pausahaan: Dimekarkeun ku Shanghai Sunway Biotéhnologi Co., Ltd.
Waktos ka pasar: Disatujuan pikeun daptar di Cina di 2005.
Indikasi: Pangobatan tumor sirah sareng beuheung, kanker ati, kanker pankréas, kanker serviks sareng kanker sanés.
Catetan: Oncorine mangrupikeun produk terapi gen virus oncolytic anu ngagunakeun adenovirus salaku véktor.Adenovirus oncolytic nu diala bisa ngayakeun réplikasi husus dina tumor kakurangan atawa gén p53 abnormal, ngabalukarkeun lisis sél tumor, kukituna maéhan sél tumor.tanpa ngaruksak sél normal.Hasil klinis nunjukeun yen Anke Rui boga kaamanan alus tur efficacy pikeun rupa-rupa tumor ganas.
(4) Glybera
Perusahaan: Dimekarkeun ku uniQure.
Waktos ka pasar: Disatujuan di Éropa dina 2012.
Indikasi: Pangobatan kakurangan lipoprotein lipase (LPLD) kalayan épisode pankreatitis parna atanapi kambuh sanajan diet lemak anu diwatesan sacara ketat.
Catetan: Glybera (alipogene tiparvovec) mangrupikeun ubar terapi gén dumasar kana AAV salaku vektor.Terapi ieu ngagunakeun AAV salaku véktor pikeun mindahkeun LPL gén terapi kana sél otot, ku kituna sél pakait bisa ngahasilkeun jumlah nu tangtu lipoprotein lipase, Ieu muterkeun hiji peran dina relieving kasakit, sarta terapi ieu éféktif pikeun lila sanggeus hiji administrasi (éfék bisa lepas salila sababaraha taun).Ubar kasebut dihapus dina 2017, sareng alesan pikeun ngahapus daptarna tiasa aya hubunganana sareng dua faktor: harga anu luhur teuing sareng paménta pasar terbatas.Biaya rata-rata pikeun pengobatan tunggal ubar saluhur 1 juta dolar AS, sareng ngan ukur hiji pasien anu ngagaleuh sareng ngagunakeunana dugi ka ayeuna.Sanajan pausahaan asuransi médis reimbursed eta pikeun 900.000 dollar AS, éta ogé beban badag pikeun parusahaan asuransi.Salaku tambahan, indikasi pikeun ubar jarang pisan, kalayan tingkat insiden sakitar 1 dina 1 juta sareng tingkat misdiagnosis anu luhur.
(5) Imligic
pausahaan: Dimekarkeun ku Amgen.
Waktos ka pasar: Dina 2015, éta disatujuan pikeun daptar di Amérika Serikat sareng Uni Éropa.
Indikasi: Perawatan lesi melanoma anu teu tiasa dileungitkeun lengkep ku bedah.
Catetan: Imlygic mangrupakeun dirobah genetik (ngahapus fragmen gén ICP34.5 na ICP47 na, sarta ngasupkeun gén GM-CSF koloni granulocyte-makrofag manusa faktor stimulasi kana virus) attenuated herpes simplex virus tipe 1 (HSV-1) virus oncolytic, terapi virus oncolytic munggaran FDA-disatujuan.Métode administrasi nyaéta suntikan intralesional.Suntikan langsung kana lesi melanoma tiasa nyababkeun beubeulahan sél tumor sareng ngaleupaskeun antigén turunan tumor sareng GM-CSF pikeun ngamajukeun réspon imun anti tumor.
(6) Luxturna
Perusahaan: Dimekarkeun ku Spark Therapeutics, anak perusahaan Roche.
Waktos ka pasar: Disatujuan ku FDA di 2017, teras disatujuan pikeun pamasaran di Éropa dina 2018.
Indikasi: Pikeun pengobatan murangkalih sareng déwasa anu kaleungitan visi kusabab mutasi dina salinan ganda gén RPE65 tapi kalayan jumlah sél rétina anu cekap.
Catetan: Luxturna mangrupikeun terapi gén dumasar AAV anu dikaluarkeun ku suntikan subretinal.Terapi gén ngagunakeun AAV2 salaku pamawa pikeun ngenalkeun salinan fungsional gén RPE65 normal kana sél rétina pasien, ku kituna sél saluyu nganyatakeun protéin RPE65 normal pikeun ngimbangan cacad protéin RPE65 sabar urang, kukituna ngaronjatkeun visi sabar urang.
(7) Zolgénsma
Perusahaan: Dimekarkeun ku AveXis, anak perusahaan Novartis.
Waktos ka pasar: Disatujuan ku FDA dina Méi 2019.
Indikasi: Pengobatan atrofi otot tulang tonggong (Spinal Muscular Atrophy, SMA) pasien di handapeun umur 2 taun.
Catetan: Zolgensma mangrupikeun terapi gen dumasar kana vektor AAV.Ubar ieu mangrupikeun hiji-hijina rencana perawatan pikeun atrofi otot tulang tonggong anu disatujuan pikeun pamasaran di dunya.kaca, mangrupakeun kamajuan milestone.Terapi gén ieu ngagunakeun véktor scAAV9 pikeun ngawanohkeun gén SMN1 normal ka penderita ngaliwatan infus intravena, ngahasilkeun protéin SMN1 normal, kukituna ngaronjatkeun fungsi sél kapangaruhan kayaning neuron motor.Sabalikna, ubar SMA Spinraza sareng Evrysdi meryogikeun dosis anu diulang dina waktos anu lami, kalayan Spinraza dikaluarkeun salaku suntikan tulang tonggong unggal opat bulan, sareng Evrysdi, ubar lisan sapopoé.
(8) Delytact
pausahaan: Dimekarkeun ku Daiichi Sankyo Company Limited (TYO: 4568).
Waktos ka pasar: Persetujuan sarat ti Kamentrian Kaséhatan, Buruh sareng Kesejahteraan Jepang (MHLW) dina Juni 2021.
Indikasi: Pikeun pengobatan glioma malignant.
Catetan: Delytact mangrupikeun produk terapi gen virus oncolytic kaopat anu disatujuan sacara global sareng produk virus oncolytic munggaran anu disatujuan pikeun pengobatan glioma ganas.Delytact mangrupikeun virus oncolytic herpes simplex tipe 1 (HSV-1) anu direkayasa genetik anu dikembangkeun ku Dr Todo sareng kolega.Delytact ngenalkeun mutasi ngahapus tambahan kana génom G207 generasi kadua HSV-1, ningkatkeun réplikasi selektif na dina sél kanker sareng induksi réspon imun anti tumor, bari ngajaga profil kaamanan anu luhur.Delytact mangrupikeun generasi katilu HSV-1 oncolytic munggaran anu ayeuna dina evaluasi klinis.Persetujuan Delytact di Jepang dumasar kana uji klinis Fase 2 panangan tunggal.Dina penderita glioblastoma kumat, Delytact patepung titik tungtung primér survival sataun, sarta hasil némbongkeun yén Delytact dipigawé hadé ti G207.Réplikasi anu kuat sareng kagiatan antitumor anu langkung luhur.Ieu mujarab dina model tumor padet kaasup payudara, prostat, schwannoma, nasopharyngeal, hepatocellular, colorectal, tumor malapah saraf periferal malignant jeung kanker tiroid.
(9) Upstaza
pausahaan: Dimekarkeun ku PTC Therapeutics, Inc. (NASDAQ: PTCT).
Waktos ka pasar: Disatujuan ku EU dina Juli 2022.
Indikasi: Pikeun kakurangan asam L-amino decarboxylase (AADC) aromatik, disatujuan pikeun pengobatan pasien umur 18 bulan sareng langkung lami.
Catetan: Upstaza™ (eladocagene exuparvovec) nyaéta terapi gén in vivo ngagunakeun tipe virus adeno-associated 2 (AAV2) salaku véktor.Pasién gering kusabab mutasi gen anu ngodekeun énzim AADC.AAV2 mawa gén cageur encoding énzim AADC.Pangaruh terapi kahontal dina bentuk santunan genetik.Sacara tiori, dosis tunggal mujarab pikeun lila.Ieu terapi gén munggaran dipasarkan langsung nyuntik kana uteuk.Otorisasi pamasaran manglaku ka sadaya 27 nagara anggota Uni Éropa, ogé Islandia, Norwégia sareng Liechtenstein.
(9) Roktavian
Perusahaan: Dimekarkeun ku BioMarin Pharmaceutical (BioMarin).
Waktos ka pasar: Disatujuan ku EU dina Agustus 2022.
Indikasi: Pikeun pengobatan pasien dewasa sareng hemofilia A parah tanpa riwayat inhibisi faktor FVIII sareng antibodi AAV5 négatip.
Catetan: Roctavian (valoctocogene roxaparvovec) ngagunakeun AAV5 salaku véktor sareng nganggo HLP promoter khusus ati manusa pikeun ngajalankeun ekspresi faktor koagulasi manusa dalapan (FVIII) kalayan domain B dihapus.Kaputusan Komisi Éropa pikeun nyatujuan pamasaran valoctocogene roxaparvovec dumasar kana data sakabéh program pangembangan klinis ubar.Di antarana, fase III percobaan klinis GENEr8-1 némbongkeun yén dibandingkeun jeung data taun saméméh enrollment, sanggeus infusion tunggal vactocogene roxaparvovec, Subjék miboga tingkat perdarahan taunan nyata handap (ABR), kirang sering pamakéan rekombinan faktor VIII (F8) olahan protéin, atawa kanaékan signifikan dina aktivitas getih F8 dina awak.Sanggeus 4 minggu perlakuan, pamakéan F8 taunan subjék 'na ABR merlukeun perlakuan anu ngurangan ku 99% na 84% masing-masing, béda anu signifikan sacara statistik (p<0.001).Propil kaamanan nguntungkeun, sareng henteu aya subjek anu ngalaman inhibisi faktor F8, malignancy, atanapi efek samping thrombotic, sareng teu aya kajadian ngarugikeun serius (SAEs) anu aya hubunganana sareng perlakuan.
3. Ubar asam nukléat leutik
(1) Vitravene
Perusahaan: Dimekarkeun babarengan ku Ionis Pharma (baheulana Isis Pharma) sareng Novartis.
Waktos ka pasar: Disatujuan ku FDA sareng EU EMA dina 1998 sareng 1999.
Indikasi: Pikeun pengobatan retinitis cytomegalovirus di penderita HIV-positip.
Catetan: Vitravene mangrupikeun ubar oligonukleotida antisense sareng ubar oligonukleotida munggaran anu disatujuan pikeun pamasaran di dunya.Dina awal pasar, paménta pasar pikeun ubar anti cytomegalovirus éta pisan urgent;lajeng alatan ngembangkeun terapi antiretroviral kacida aktif, jumlah kasus cytomegalovirus turun sharply.Alatan paménta pasar low, ubar dirilis dina 2002 jeung 2006 Ditarikna di nagara Uni Éropa jeung AS.
(2) Macugen
pausahaan: Co-dimekarkeun ku Pfizer na Eyetech.
Waktos ka pasar: Disatujuan pikeun daptar di Amérika Serikat dina 2004.
Indikasi: Pikeun pengobatan degeneration macular nu patali umur neovascular.
Catetan: Macugen mangrupikeun ubar oligonukleotida anu dirobih pegylated anu tiasa nargétkeun sareng ngabeungkeut faktor pertumbuhan endothelial vaskular (VEGF165 isoform), sareng dikaluarkeun ku suntikan intravitreal.
(3) Defitelio
pausahaan: Dimekarkeun ku Jazz.
Waktos ka pasar: Disatujuan ku Uni Éropa dina 2013, sareng disatujuan ku FDA dina Maret 2016.
Indikasi: Pikeun pengobatan kasakit occlusive venule hépatik pakait sareng disfungsi ginjal atawa pulmonal sanggeus cangkok sél stém hematopoietic.
Catetan: Defitelio mangrupikeun ubar oligonukleotida, campuran oligonukleotida sareng sipat plasmin.Ieu ditarik dina 2009 alesan komérsial.
(4) Kynamro
pausahaan: Co-dimekarkeun ku Ionis Pharma jeung Kastle.
Waktos ka pasar: Disatujuan di Amérika Serikat salaku ubar yatim di 2013.
Indikasi: Pikeun pengobatan adjuvant hypercholesterolemia familial homozygous.
Catetan: Kynamro mangrupikeun ubar oligonukleotida antisense, oligonukleotida antisense anu nargétkeun apo B-100 mRNA manusa.Kynamro dikaluarkeun salaku 200 mg subcutaneously saminggu sakali.
(5) Spinraza
Perusahaan: Dimekarkeun ku Ionis Pharmaceuticals.
Waktos ka pasar: Disatujuan ku FDA dina bulan Désémber 2016.
Indikasi: Pikeun pengobatan atrofi otot tulang tonggong (SMA).
Catetan: Spinraza (nusinersen) mangrupikeun ubar oligonukleotida antisense.Spinraza bisa ngarobah splicing RNA gén SMN2 ku cara ngabeungkeut situs splicing of SMN2 exon 7, kukituna ngaronjatkeun produksi protéin SMN fungsi pinuh.Dina Agustus 2016, BIOGEN Corporation ngalaksanakeun pilihanna pikeun meunangkeun hak global Spinraza.Spinraza mimiti uji klinis kahijina di manusa dina 2011. Dina ngan 5 taun, éta disatujuan ku FDA di 2016, reflecting pangakuan pinuh FDA ngeunaan efficacy na.Ubar ieu disatujuan pikeun pamasaran di Cina dina April 2019. Sakabéh siklus persetujuan Spinraza di Cina kirang ti 6 bulan.Geus 2 taun 2 bulan saprak Spinraza munggaran disatujuan di Amérika Serikat.Sapertos blockbuster asing panyakit langka ubar anyar aya dina Laju Listing di Cina geus pisan gancang.Ieu ogé disababkeun ku "Bewara ngeunaan Pelepasan Daptar Kahiji Narkoba Anyar Luar Negeri Dibutuhkeun Urgent pikeun Panaliti Klinis" dikaluarkeun ku Pusat Evaluasi Narkoba dina 1 Nopémber 2018, anu kalebet dina angkatan munggaran 40 ubar anyar asing konci pikeun ulasan gancangan, sareng Spinraza rengking.
(6) Exondys 51
pausahaan: Dimekarkeun ku AVI BioPharma (engké diganti Sarepta Therapeutics).
Waktos ka pasar: Disatujuan ku FDA dina Séptémber 2016.
Indikasi: Pikeun pengobatan Duchenne muscular dystrophy (DMD) kalawan mutasi gén DMD dina exon 51 skipping gén.
Catetan: Exondys 51 mangrupikeun ubar oligonukleotida antisense.Oligonukleotida antisense tiasa ngabeungkeut kana posisi exon 51 tina pre-mRNA gén DMD, hasilna formasi mRNA dewasa.Eksisi, sahingga sawaréh ngabenerkeun pigura bacaan mRNA, ngabantosan pasien pikeun nyintésis sababaraha bentuk dystrophin fungsional anu langkung pondok tibatan protéin normal, ku kituna ningkatkeun gejala pasien.
(7) Tegsedi
Perusahaan: Dimekarkeun ku Ionis Pharmaceuticals.
Waktos ka pasar: Disatujuan ku Uni Éropa pikeun pamasaran dina Juli 2018.
Indikasi: Pikeun pengobatan turunan transthyretin amyloidosis (hATTR).
Catetan: Tegsedi mangrupikeun ubar oligonukleotida antisense anu nargétkeun mRNA transthyretin.Ieu mangrupikeun ubar anu disatujuan munggaran di dunya pikeun pengobatan hATTR.Métode administrasi nyaéta suntikan subkutan.Ubar ieu ngirangan produksi protéin ATTR ku nargétkeun mRNA transthyretin (ATTR), sareng gaduh rasio kauntungan-resiko anu hadé dina pengobatan ATTR.Sanes tahap panyakit atanapi ayana cardiomyopathy henteu relevan.
(8) Onpattro
Perusahaan: Dimekarkeun babarengan ku Alnylam sareng Sanofi.
Waktos ka pasar: Disatujuan pikeun daptar di Amérika Serikat dina 2018.
Indikasi: Pikeun pengobatan turunan transthyretin amyloidosis (hATTR).
Catetan: Onpattro mangrupikeun ubar siRNA anu nargétkeun mRNA transthyretin, anu ngirangan produksi protéin ATTR dina ati sareng akumulasi deposit amyloid dina saraf periferal ku nargétkeun mRNA transthyretin (ATTR)., kukituna ngaronjatkeun jeung relieving gejala panyakit.
(9) Givlaari
pausahaan: Dimekarkeun ku Alnylam Corporation.
Waktos ka pasar: Disatujuan ku FDA dina bulan Nopémber 2019.
Indikasi: Pikeun pengobatan porphyria hépatik akut (AHP) dina déwasa.
Catetan: Givlaari mangrupakeun ubar siRNA, ubar siRNA kadua disatujuan pikeun pamasaran sanggeus Onpattro.Ubar kasebut dikaluarkeun sacara subkutan sareng nargétkeun mRNA pikeun degradasi protéin ALAS1.Perawatan Givlaari bulanan tiasa sacara signifikan sareng terus-terusan ngirangan tingkat ALAS1 dina ati, ku kituna ngirangan tingkat ALA neurotoksik sareng PBG kana kisaran normal, ku kituna ngaleungitkeun gejala panyakit pasien.Data nunjukkeun yén pasien anu dirawat kalayan Givlaari ngagaduhan pangurangan 74% dina jumlah panyawat panyakit dibandingkeun sareng grup plasebo.
(10) Vyondys53
Perusahaan: Dimekarkeun ku Sarepta Therapeutics.
Waktos ka pasar: Disatujuan ku FDA dina bulan Désémber 2019.
Indikasi: Pikeun pengobatan penderita DMD kalawan dystrophin gén exon 53 mutasi splice.
Catetan: Vyondys 53 mangrupikeun ubar oligonukleotida antisense.Ubar oligonukleotida nargétkeun prosés splicing prékursor mRNA dystrophin.Dina prosés teu langsung tina prékursor mRNA dystrophin, Exon 53 éksternal ieu sawaréh spliced kaluar, nyaéta henteu hadir dina mRNA dewasa, sarta dirancang pikeun ngahasilkeun protéin dystrophin truncated tapi masih fungsi, kukituna ngaronjatkeun kapasitas latihan di penderita.
(11) Waylivra
Perusahaan: Dimekarkeun ku Ionis Pharmaceuticals sareng cabangna Akcea Therapeutics.
Waktos ka pasar: Disatujuan ku Badan Obat Éropa (EMA) dina Méi 2019.
Indikasi: Salaku terapi adjunctive kana diet anu dikontrol dina pasien sawawa sareng sindrom chylomicronemia familial (FCS).
Catetan: Waylivra mangrupikeun ubar oligonukleotida antisense, anu mangrupikeun ubar munggaran anu disatujuan pikeun pengobatan FCS di dunya.
(12) Leqvio
pausahaan: Dimekarkeun ku Novartis.
Waktos ka pasar: Disatujuan ku EU dina bulan Désémber 2020.
Indikasi: Pikeun pengobatan hypercholesterolemia primér sawawa (famili heterozygous sareng non-familial) atanapi dislipidemia campuran.
Catetan: Leqvio mangrupikeun ubar siRNA anu nargétkeun PCSK9 mRNA.Éta mangrupikeun terapi siRNA nurunkeun kolesterol (LDL-C) munggaran di dunya.Métode administrasi nyaéta suntikan subkutan.Ubar ieu dianggo ku gangguan RNA pikeun nurunkeun tingkat protéin PCSK9, anu salajengna nurunkeun tingkat LDL-C.Data klinis nunjukkeun yén Leqvio tiasa ngirangan LDL-C sakitar 50% dina pasien anu tingkat LDL-C henteu tiasa diréduksi ka tingkat target sanaos dosis statin anu ditolerir maksimal.
(13) Oxlumo
Perusahaan: Dimekarkeun ku Alnylam Pharmaceuticals.
Waktos ka pasar: Disatujuan ku EU dina Nopémber 2020.
Indikasi: Pikeun pengobatan hyperoxaluria primér tipe 1 (PH1).
Catetan: Oxlumo mangrupikeun ubar siRNA anu nargétkeun mRNA asam hidroksi oksidase 1 (HAO1), anu dikaluarkeun sacara subkutan.Ubar ieu dikembangkeun nganggo téknologi konjugasi ESC-GalNAc kimia stabilisasi panganyarna Alnylam, anu ngamungkinkeun siRNA anu dikaluarkeun sacara subkutan kalayan kegigihan sareng khasiat anu langkung ageung.Ubar nargétkeun dégradasi atanapi inhibisi asam hidroksi oksidase 1 (HAO1) mRNA, ngirangan tingkat glikolat oksidase dina ati, teras ngonsumsi substrat anu dipikabutuh pikeun produksi oksalat sareng ngirangan produksi oksalat pikeun ngontrol kamajuan panyakit sareng ningkatkeun gejala panyakit dina pasien.
(14) Viltepso
Perusahaan: Dimekarkeun ku NS Pharma, anak perusahaan Nippon Shinyaku.
Waktos ka pasar: Disatujuan ku FDA dina Agustus 2020.
Indikasi: Pikeun pengobatan Duchenne muscular dystrophy (DMD) kalawan mutasi gén DMD dina exon 53 skipping gén.
Catetan: Viltepso mangrupikeun ubar phosphorodiamide morpholino oligonucleotide.Ubar oligonukleotida ieu tiasa ngabeungkeut kana posisi exon 53 tina pre-mRNA gén DMD, nyababkeun formasi mRNA dewasa.Exon sawaréh dipiceun, ku kituna sawaréh ngabenerkeun pigura bacaan mRNA, ngabantosan pasien nyintésis sababaraha bentuk fungsional dystrophin anu langkung pondok tibatan protéin normal, ku kituna ningkatkeun gejala pasien.
(15) Amvuttra (vutrisiran)
Perusahaan: Dimekarkeun ku Alnylam Pharmaceuticals.
Waktos ka pasar: Disatujuan ku FDA dina Juni 2022.
Indikasi: Pikeun pengobatan amyloidosis transthyretin turunan sawawa sareng polyneuropathy (hATTR-PN).
Catetan: Amvuttra (Vutrisiran) mangrupikeun ubar siRNA anu nargétkeun transthyretin (ATTR) mRNA, anu dikaluarkeun ku suntikan subkutan.Vutrisiran dirancang dumasar kana Alnylam's Enhanced Stabilisation Chemistry (ESC) -GalNAc platform pangiriman conjugated kalawan ngaronjat potency jeung stabilitas métabolik.Persetujuan terapi dumasar kana data 9-bulan tina studi klinis Fase III na (HELIOS-A), kalayan hasil sacara umum nunjukkeun yén terapi ningkatkeun gejala hATTR-PN, kalayan langkung ti 50% pasien ngabalikeun atanapi ngeureunkeun kamajuan.
4. Ubar terapi gén séjén
(1) Rexin-G
Perusahaan: Dimekarkeun ku Epeius Biotech.
Waktos ka pasar: Disatujuan ku Administrasi Pangan sareng Narkoba Filipina (BFAD) dina 2005.
Indikasi: Pikeun pengobatan kangker canggih anu tahan ka kémoterapi.
Catetan: Rexin-G mangrupikeun suntikan nanopartikel anu sarat gen.Ieu ngenalkeun gén mutant cyclin G1 kana sél target ngaliwatan véktor retroviral pikeun sacara khusus maéhan tumor padet.Métode administrasi nyaéta infus intravena.Salaku ubar target tumor anu aktip milarian sareng ngancurkeun sél kanker métastatik, éta ngagaduhan pangaruh anu tangtu pikeun pasien anu henteu épéktip ngalawan ubar kanker sanés, kalebet biologis anu dituju.
(2) Neovasculgen
Perusahaan: Dimekarkeun ku institut sél stém Asasi Manusa.
Waktu daptar: Disatujuan pikeun daptar di Rusia dina 7 Désémber 2011, teras didaptarkeun di Ukraina di 2013.
Indikasi: Pikeun pengobatan panyakit arteri periferal, kalebet iskemia dahan parna.
Catetan: Neovasculgen mangrupikeun terapi gén dumasar-plasmid DNA dimana gén faktor pertumbuhan endothelial vaskular (VEGF) 165 diwangun dina tulang tonggong plasmid sareng diinfuskeun ka pasien.
(3) Collategene
Perusahaan: Dimekarkeun babarengan ku Universitas Osaka sareng perusahaan modal usaha.
Waktu daptar: Disatujuan ku Kamentrian Kaséhatan, Buruh sareng Kesejahteraan Jepang pikeun daptar dina Agustus 2019.
Indikasi: Pangobatan iskemia ekstrimitas handap parah.
Catetan: Collategene mangrupikeun terapi gén dumasar plasmid, ubar terapi gén asli Jepang munggaran anu diproduksi ku AnGes.Komponén utama ubar ieu nyaéta plasmid taranjang anu ngandung sekuen gén faktor pertumbuhan hépatosit manusa (HGF).Upami obat disuntikkeun kana otot anggota awak handap, HGF anu dikedalkeun bakal ngamajukeun pembentukan pembuluh darah anyar di sekitar pembuluh darah anu terhalang.Uji klinis parantos mastikeun efektivitasna dina ningkatkeun borok.
TUNGTUNG
waktos pos: Nov-10-2022